هیدرازین صنعتی و کاربرد های آن

هیدرازین (Hydrazine) یک ترکیب شیمیایی که از نیتروژن و هیدروژن تشکیل میشود ، اولین بار در سال 1889 میلادی توسط شیمیدان و استاد دانشگاه هایدلبرگ آلمان به نام تئودور کورتیوس شناخته شد اما نتوانست آن را ثابت کند اما سرانجام در سال 1907 ، شیمی دان آلمانی به نام فردریش راشیگ با فرایند Olin-Rasching توانست وجود این ماده را ثابت کند . هیدرازینیوم هیدروکسید که نام دیگر هیدرازین است دریک واکنش چند مرحله ایی از هیدروژن پراکسید، استون و آمونیاک به دست می آید به همین دلیل آن را میتوان در دسته ای از مواد آلی قرار داد . این ماده شیمیایی با اینکه که فرمول مولکولی ساده ایی دارد ولی با داشتن چند خصوصیات فیزیکی و شیمیایی ، هیدرازین را به یک ماده پر کاربرد و مفید در صنعت تبدیل کرده است که در مخمرها ، قارچ ها ، میکروارگانسیم ها و باکتری ها تولید میشود . در ادامه مقاله به کاربردهای هیدرازین در صنعت اشاره میکنیم .
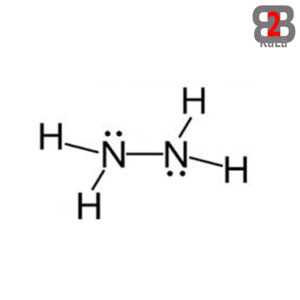
N2H4 آرایش اتمی هیدرازین صنعتی
تولید هیدرازینیوم هیدروکسید
این ترکیب به سه روش ساخته میشود:
1-فرایند راشینگ
اولین و اصلی ترین روش تولید این ماده ، Raschig process است که آمونیاک (NH3)با کلروآمین (C7H7ClNO2SNa) و هیپوکلریت سدیم (NaClO) اکسید میشود و کلرآمین با آمونیاک اضافی موجود در نمونه و سدیم هیدروکسید(NaOH) واکنش داده و هیدرازین هیدرات (N2H4)یا به عبارت دیگر هیدروزین و نمک سدیم کلراید(NaCl) را تشکیل میدهند.
2-فرایند کتازین
روش کتازین نیز نوعی روش راشینگ است که امروزه هیدرازین بیشتر به روش دوم تولید میشود . بدین صورت که آمونیاک با کلر یا کلرو آمین در حضور استون (C3H6O) که معمولا به عنوان یک کتون آلیفاتیک از آن استفاده میکنند ، واکنش داده و اکسید میشود . در نهایت کتازین تولید شده با هیدرازینیوم هیدروکسید ، هیدرولیز (واکنش شیمیایی که ترکیب شیمیایی با آب واکنش داده و و مولکول H2O رابه یون های هیدروژن (+H) و هیدروکسیل (‾OH) تبدیل میکند) میشود.
3-فرایند پراکسید
همانظور که از نامش پیداست ، در این روش برای اکسید کردن آمونیاک در حضور کتون از هیدروژن پراکسید(H2O2) استفاده میکنند.
خصوصیات هیدرازین درصنعت
- بسیار سمی ، فرار و قابل پخش در محیط با سرعت بالا ، سرطان زا و خطرناک است اما ترکیب آن با آب (N2H4.XH2O) که به آن هیدرازین هیدراته میگویند ، خطرناک نیست .
- هیدرازین یک ترکیب باز شیمیایی بسیار واکنش دهنده و کاهنده در سنتز آلی است .
- به دلیل نزیک بودن دامنه دمایی به آب ، دامنه چگالی شیبه به هم دارند .
- این ماده با اینکه 15 برابر ضعیف تراز آمونیاک است اما بوی مشابهی به آمونیاک دارد که بویی نافذ و تند است .
- نوع آبدار ماده هیدرازین که هم به شکل محلول ساده است و هم به صورت کاتالیزشده است را برای جایگزین کردن هیدروکسید سدیم به عنوان ماده معدنی استفاده میکنند .
- هنگام گرم شدن در مرحله تجزیه ، بخارهای سمی هیدروژن ، اکسید نیتروژن و آمونیاک آزاد میشوند که منجر به انفجار و آتش سوزی میشوند .
- در تماس بودن این ماده با طلا، برنج ، کادمیوم ، فولاد ضد زنگ باعث تجزیه شیمیایی آن ماده میشود .
جدول مشخصات هیدرازینیوم هیدروکسید
مشخصات مهم هیدرازین صنعتی که در زیر اشاره شده است ، عبارتند از:
| فرمول شیمیایی | NH2NH2 |
| فرمول مولکولی | N2H4 |
| جرم مولی | 32.04gr/mol |
| خصوصیات | بی رنگ،بوی تند، روغنی، محلول در آب، قابل اشتعال |
| نقطه ذوب | 51.7°C- |
| نقطه جوش | 120.1°C |
| چگالی در دمای 20 درجه سانتی گراد | 1.03gr/ml |
غلظت های هیدرازین و کاربرد های آن در صنعت
- هیدرازینیوم هیدروکسید با غلظت % 100 در صنعت پرشکی در ساخت داروهای ضد سرطان ، ضد افسردگی ، ضدقارچ ، ضدحساسیت ، ضد پارکینسون ، ضد توبولار ، ضد خونریزی ، ضد میگرن و ادرار آور و… به کار میرود .
- هیدرازین % 80 می تواند به عنوان احیا کننده در سموم دفع افات ، ماده رنگ کننده ، مواد شیمیایی عکاسی ، در حشره کش ها و آنتی اکسیدان ها و رنگ های نساجی و… به کار روند .
- هیدرازین هیدرات %55 که در تولید فرمولاسیون آب به کار میرود ، به عنوان پاک کننده و محافظ اکسیژن در تصفیه آب دیگ بخار و آب شیرین مورد استفاده قرار میگیرد .
- از این ترکیب شیمیایی با غلظت %24 در ساخت فوم های پلیمری ، کاتالیزورهای پلیمریزاسیون و گاز مورد استفاده در کیسه های هوا مانند ایربگ خودروها استفاده میکنند .
- برای جلوگیری از خوردگی تجهیزات پالایشگاهی و نیروگاهی از این ماده استفاده میکنند .
- برای پیش سازهای گازی و برای سوخت های فضاپیماها و موشک ها به دلیل همراه بودن با متانول،که اولین بار در جنگ جهانی دوم استفاده شده بود نیز استفاده میکنند چرا که با داشتن خاصیت گرمازا با اکسیژن واکنش داده وگاز N2 و H2O را تولید میکند و به همین دلیل است هیدرازین را جایگزین امن تری به جای گازهیدروژن میدانند .
علت استفاده از هیدرازین در سوخت موشک به جای آمونیاک
هیدرازین از 2 اتم نیتروژن و 4 اتم هیدروژن تشکیل شده است اما آمونیاک از 1 اتم نیتروژن و 3 اتم هیدروژن تشکیل شده است پس میتوان گف که هیدرازین از مشتق های آمونیاک است و همچنین به دلیل با دوام بودن در یک مخزن تمیز در مدت زمان طولانی و چون دچار هیچ گونه تغییرات شیمیایی در مدت زمان طولانی نمیشود ، این ترکیب را به عنوان سوخت پاک یاد میکنند برای مثال ، این ترکیب در اواسط دهه 90 در ماهواره هایی به نام Block 1 استفاده میشد ، امروزه نیز همان ماهواره بدون از دست دادن پایداری خود همچنان کار میکند .
عوارض هیدرازینیوم هیدروکسید و راه های جلوگیری از آن
- تماس چشم ها با این ترکیب ، باعث قرمزی چشم ، درد ، ورم و باعث سوختگی های عمیق چشم و… میشود که برای جلوگیری از این خطرات باید از عینک های مخصوص ، ماسک، روپوش و دستکش استفاده کنید و در صورت تماس با چشم حتما 20 دقیقه با آب فراوان شستشو دهید و در اسرع وقت به پزشک مراجعه کنید .
- از بلعیدن و استنشاق این ماده خیلی سمی پرهیز کنید و در صورت بلعیدن فورا دهان خود را شستشو دهید و درسریع ترین زمان ممکن به پزشک مراجعه کنید .
- لازم به ذکر است محلول های دارای این ترکیبات به قدری خورنده هستند که به راحتی میتوانند باعث خوردگی پوست شوند و همچنین قرار گرفتن در مقابل این ترکیب در غلظت های بالا و در مواقع سوختن این ماده شیمیایی باعث تحریک و سوزش بینی ، چشم گلو و باعث سردرد ، حالت تهوع ، تشنج وکما میشود و در بعضی مواقع به کلیه ها ، سیستم عصبی مرکزی (CNS) و کبد ، آسیب جدی میرساند.
کشورهای تولید کننده هیدرازین صنعتی
در قاره اروپا ، کشور آلمان بیشترین تولید کننده هیدرازین را به خود اختصاص داده است و بعد آن کشورهای فرانسه سپس بریتانیا و ایتالیا بزرگ ترین تولید کننده ها برای این ماده هستند اما در قاره آمریکای شمالی ، ایالات متحده آمریکا بیشترین سهم را تولید میکند و کشور چین نیز توانست در آسیا و اقیانوس تولید این ترکیب شیمیایی بپردازد .
خطر |
|
| H226 | مابع و بخار قابل اشتعال |
| H301 | سمی بودن در صورت بلعیدن |
| H311 | سمی بودن در تماس با پوست |
| H314 | موجب سوختگی شدید پوست و آسیب رساندن به چشم |
| H317 | ممکن است باعث حساسیت پوستی شود . |







